ゾルゲンスマはCL-101試験、LT-001試験、CL-303試験、CL-304試験及びCL-102試験の計5試験の結果を基に承認された。CL-101試験以外の4試験は承認の時点では試験進行中であり、臨床試験の結果は、SMN2遺伝子のコピー数が2のⅠ型SMA患者を対象としたCL-101試験(承認時評価資料)について記載した。本品は希少疾病用再生医療等製品であるため、参考として実施中のCL-101試験終了後の長期安全性フォローアップを目的としたLT-001試験(承認時参考資料)の中間解析結果も記載した。
また、日本人患者3例が参加した発症前SMA 患者(SMN2遺伝子のコピー数が2又は3)を対象としたCL-304試験(承認時参考資料)は2021年に完了しており、その最終結果も記載した。

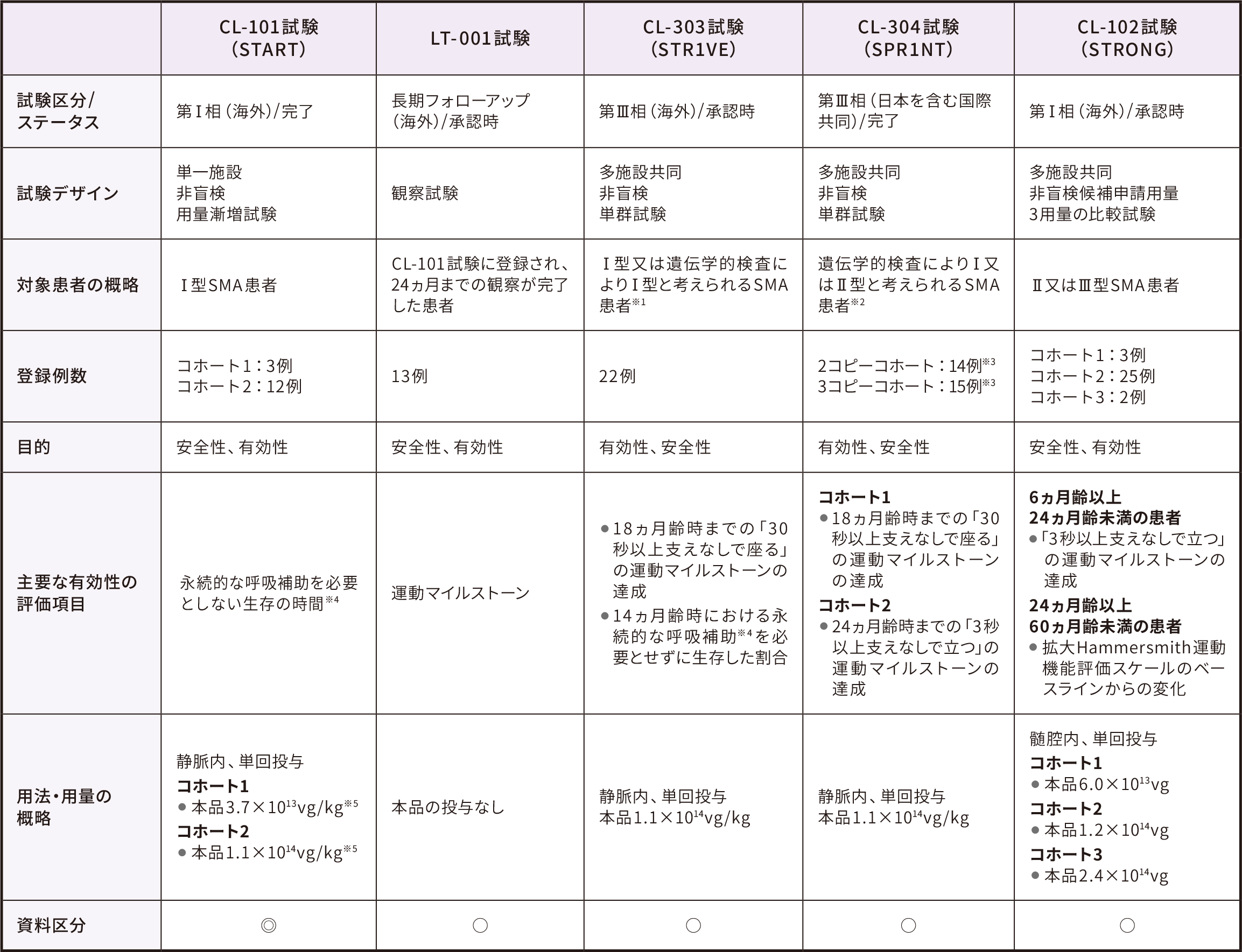
◎:承認時評価資料、〇:承認時参考資料
※ 1 :2018年6月8日までに登録を完了した。
※ 2 :治験実施計画書改訂で、Ⅲ型SMA(SMN2遺伝子コピー数が4)の患者は登録基準から削除された。
※ 3 :コホート1にはSMN2遺伝子コピー数が2のⅠ型SMA 患者、コホート2にはSMN2遺伝子コピー数が3のⅡ型SMA患者が登録された。
※ 4 :永続的な呼吸補助は、14日以上連続して16時間/日以上の呼吸補助(非侵襲的な呼吸補助を含み、可逆的な急性疾患及び周術期の呼吸補助を除く)を必要とする状態、と定義した。
※ 5 :初期開発段階の定量ポリメラーゼ連鎖反応(qPCR)法による測定では、コホート1は6.7×1013vg/kg、コホート2は2.0×1014vg/kgであったが、より正確な液滴デジタルポリメラーゼ連鎖反応(ddPCR)法で測定したところ、それぞれ、3.7×1013vg/kg、1.1×1014vg/kgと確認された。